| Treffer: 249 |
|
 A00a A00a
Experiment
| Umgang mit dem Gasbrenner

Wichtige Grundübungen: Handhaben einer leuchtenden und einer rauschen Flamme. Erfahren der Temperaturverteilung und Verdampfen einer Kleinen Wassermenge im Reagnezgllas. | 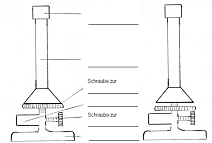 |
|
 A00c A00c
Experiment
| Glasbearbeitung im Unterricht

Wichtige Grundübungen
:Glasrohr abtrennen, stumpf schmelzen, ziehen einer Pipette oder Kapillare, blasen einer Kugel, Boden machen, ansetzen und zusammenschmelzen Oliven machen etc. | |
|
 A01 A01
Experiment
LowCost und Medizin-Technik
Experiment-Video
| "Wasser-Wasser" - Qualitative Analyse

Wasserdampf wird unter Luftausschluss mit Magnesium umgesetzt. Das bei der Reaktion entstehende Gas wird mit der Knallgasprobe untersucht. Zum Teil mit Material der Fa. Zinsser. |  |
|
 A01a A01a
Experiment
LowCost und Medizin-Technik
Experiment-Video
| "Wasser-Wasser" - Qualitative Analyse Reagenzglasvariante

Wasserdampf wird unter Luftausschluss mit Magnesium umgesetzt. Das bei der Reaktion entstehende Gas wird mit der Knallgasprobe untersucht. Experiment im Reagenzglas!! |  |
|
 A01b A01b
Experiment
LowCost und Medizin-Technik
| Wasser - Qualitative Analyse - Elektrolyse

Verdünnte Kalilauge wird an zwei Eisenelektroden in getrennten Gefäßen elektrolysiert. Die entstehenden Gase Wasserstoff und Sauerstoff verdrängen dabei ein entsprechendes Volumen Kalilauge aus den Elektrolysiergefäßen und können nachgewiesen werden. |  |
|
 A01d A01d
Experiment
LowCost und Medizin-Technik
All-Chem-Misst
| Dichteanomalie des Wassers

Die Veränderung der Dichte von Wasser bei Änderung der Temperatur lässt sich mit einfachen Mitteln messen. Dazu wird die Volumenänderung in Abhängigkeit von der Temperatur gemessen. Die Daten werden mit Microsoft EXCEL ausgewertet. |  |
|
 A02 A02
Experiment
LowCost und Medizin-Technik
Experiment-Video
| Wasser: Qualitative Synthese aus Wasserstoff

Wasserstoff wird kontrolliert in Luft verbrannt und das Verbrennungsprodukt mit WATESMO- Papier untersucht. |  |
|
A02a
Experiment
Experiment-Video
| Wasser: Synthese aus Wasserstoff und Sauerstoff

Wasserstoff wird in Sauerstoffatmosphäre verbrannt und das Verbrennungsprodukt kondensiert, aufgefangen und mit WATESMO- Papier untersucht. |  |
|
 A02c A02c
Experiment
LowCost und Medizin-Technik
| Qualitative Synthese von Wasser - Die wütende Kaffeedose

Es wird untersucht ob Wasserstoff mit Sauerstoff reagiert:
V2. Reaktion von Wasserstoff mit Luft (gebremster Sauerstoff) in der "Kaffeedose".
| |
|
 A03 A03
Experiment
LowCost und Medizin-Technik
Selbstbau
Selbstbau-Video
Experiment-Video
| Wasser: Halbquantitative Synthese

In einen abgedichteten Schlauch werden verschiedene Volumina Wasserstoff und Sauerstoff gemischt. Das Gemisch wird durch einen elektrischen Funken gezündet. Das evtl. Restgas wird nach Wasserstoffzugabe erneut mit einem Zündversuch getestet. |  |
|
 A03a A03a
Experiment
LowCost und Medizin-Technik
Selbstbau
| Quantitative Wasserdampfsynthese im Spritzeneudiometer

In einer für hohe Temperaturen geieigneten Spritze werden verschiedene Volumina Wasserstoff und Sauerstoff gemischt. Das Gemisch im Trockenschrank auf über 100°C erhitzt und dann durch einen elektrischen Funken gezündet. Das evtl. Restgas wird nach Wasserstoffzugabe erneut mit einem Zündversuch getestet. |  |
|
 A02b A02b
Experiment
LowCost und Medizin-Technik
| Qualitative Synthese von Wasser - Vorversuche

In drei Phasen wird untersucht ob Wasserstoff mit Sauerstoff reagiert:
V1. Anzünden von Wasserstoff-Bläschen
V2. Reaktion von Wasserstoff mit Luft (gebremster Sauerstoff) in der "Kaffeedose".
V3. Anzünden von Knallgas-Bläschen
|  |
|
 A04 A04
Experiment
LowCost und Medizin-Technik
Selbstbau
| Sauerstoffanalyse der Luft

Der Sauerstoffanteil der Luft wird durch die Reaktion mit Kupfer zu festem Kupferoxid gebunden. |  |
|
 A05a A05a
Experiment
LowCost und Medizin-Technik
| 1. Brennen von Kalk

Durch die Kleinheit der Apparatur wird es möglich mit dem Bunsenbrenner die für das Kalkbrennen nötige Temperatur zu erreichen |  |
|
 A05b A05b
Experiment
LowCost und Medizin-Technik
| 2. Löschen von Branntkalk

Im AK SÜS lässt sich leicht zeigen, dass das Löschen von Kalk stark exotherm ist. |  |
|
 A05c A05c
Experiment
LowCost und Medizin-Technik
Experiment-Video
| 3. Abbinden von Löschkalk

Im AK SÜS lässt sich leicht zeigen, dass gelöschter Kalk mit Kohlenstoffdioxid reagiert. |  |
|
A05g
Experiment
| Kohlenstoffdioxid löscht Feuer

Durch "Umgießen" von Kohlenstoffdioxid und mit der Feuertreppe wird die Löscheigenschaft des Gases erfahren. |  |
|
 A05h A05h
Experiment
LowCost und Medizin-Technik
| Herstellung von CO2-Trockeneis

Aus einer Sodapatrone kann ein klein wenig Trockeneis erhalten werden. |  |
|
 A05j A05j
Experiment
LowCost und Medizin-Technik
| Löslichkeit von CO2 in Wasser - Lösegleichgewicht

Kohlenstoffdioxid wird in Wasser gelöst und die Druckabhängigkeit untersucht. |  |
|
 A06 A06
Experiment
LowCost und Medizin-Technik
Selbstbau
Experiment-Video
| Nachweis von Kohlenstoffdioxid in der Atemluft

Mit zwei Rückschlagventilen wird eine für Schüler sichere „Atemmaschine“ aufgebaut, mit der Kohlenstoffdioxid in der Atemluft nachgewiesen werden kann. |  |
|
 A07 A07
Experiment
LowCost und Medizin-Technik
Selbstbau
Experiment-Video
| Einfache Gasherstellung

Gaserzeugung mit Medizintechnik-Teilen |  |
|
 A08 A08
Experiment
LowCost und Medizin-Technik
Selbstbau
Selbstbau-Video
Experiment-Video
| Bestimmung der Dichte/ Molmase von Gasen

Auf einer Milligrammwaage wird eine speziell präparierte Spritze zweimal gewogen: Einmal mit Vakuum und einmal mit dem zu untersuchenden Gas. Wichtig: Der Auftrieb ist bei beiden Massebestimmungen genau der gleiche. |  |
|
 A08a A08a
Experiment
LowCost und Medizin-Technik
| Bestimmung der molaren Masse von Magnesium

Magnesium wird mit Salzsäure umgesetzt. Aus dem Volumen des entstehenden Wasserstoffs und dem Stoffmengenverhältnis wird die molare Masse bestimmt. |  |
|
 A09a A09a
Experiment
LowCost und Medizin-Technik
Experiment-Video
| Ammoniak-Springbrunnen

Durch Zugabe von Wasser zu einem Gemisch aus Ammioumchlorid und festem Natriumhydroxid wird Ammoniakgas hersgestellt. Der gefüllte Kolben wird dann mit einer Düse versehen und kopfüber in mit Bromthymolblau angefärbtes Wasser gestellt |  |
|
 A09b A09b
Experiment
LowCost und Medizin-Technik
Experiment-Video
| Chlorwasserstoff-Springbrunnen

Durch Erhitzen von konzentrierter Salzsäure wird Chlorwasserstoffgas ausgetrieben. Der gefüllte Kolben wird dann mit einer Düse versehen und kopfüber in mit Bromthymolblau angefärbtes Wasser gestellt |  |
|
 A10 A10
Experiment
LowCost und Medizin-Technik
| Herstellung und Eigenschaften von Chlor

Mit HMT-Teilen der Fa. Zinsser wird in einer "sicheren" Apparatur Chlor aus Kaliumpermanganat und Salzsäure hergestellt. Die Wirkung des Chlors auf farbige Blätter und die Wirkung der Aktivkohle wird getestet. Alternativ kann die „stille Reaktion“ mit elementarem Natrium beobachtet werden |  |
|
 A11 A11
Experiment
LowCost und Medizin-Technik
Selbstbau
| Beobachtung der Ionenwanderung

In der AK- „Ionenwanderungskammer“ werden Salzsäure bzw. Natronlauge auf ein Indikatorpapier getüpfelt. Das Indikatorpapier wird angefeuchtet und an eine Gleichspannungsquelle angeschlossen: Aus den Wanderungsrichtung kann auf das Vorzeichen der Ladung der farbgebenden Ionen geschlossen werden. |  |
|
 A12 A12
Experiment
LowCost und Medizin-Technik
Selbstbau
Experiment-Video
| Feuer&Flamme: Benzinexplosion im Filmdöschen

Benzin wird in einer präparierten Filmdose "vergast". Das Gemsich lässt sich zünden. (Leider werden Filmdosen immer rarer) |  |
|
 A13 A13
Experiment
LowCost und Medizin-Technik
Selbstbau
Experiment-Video
| Feuer&Flamme: Feuerzeuggas-Rakete

Sehr wirkungsvoller Versuch für den Aussenbereich |  |
|
 A13a A13a
Experiment
LowCost und Medizin-Technik
| Feuerzeuggas(Butangas)verflüssigung durch Druck

Feuerzeuggas (besser: n- Butan) wird in einer Spritze kräftig zusammen gedrückt. Ist der Schüler stark genug, wird es verflüssigt. Danach wird durch Entspannen die Flüssigkeit wieder gasförmig. Bei gutem Willen kann man die Temperaturänderung fühlen. |  |
|
 A13b A13b
Experiment
LowCost und Medizin-Technik
| Feuerzeuggas(Butangas)verflüssigung durch Temperatur

Feuerzeuggas (besser: n- Butan) wird in einer Spritze mit Eis gekühlt. Ist die Kältemischung gut genug, lässt sich das Gas fast ohne Druck verflüssigen. Beim Erwärmen wird die Flüssigkeit wieder gasförmig. |  |
|
 A14a A14a
Experiment
LowCost und Medizin-Technik
Experiment-Video
| Feuer&Flamme: Wachsexplosion

Versuch aus der Reihe Feuer und Flamme:
Heißes Wachs wird mit kaltem Wasser angezündet. |  |
|
 A14b A14b
Experiment
Experiment-Video
| Feuer&Flamme: Entflammen von Wachs

Versuch aus der Reihe Feuer und Flamme:
Wachs wird erhitzt und dabei wird immer wieder versucht, ob es brennt. |  |
|
 A14c A14c
Experiment
Experiment-Video
| Feuer&Flamme: Weitere Versuche zur Kerze

Versuch aus der Reihe Feuer und Flamme:
Entflammen von unverbranntem Wachsdampf, Überblasen einer Flamme, Tochterflamme |  |
|
 A14d A14d
Experiment
Experiment-Video
| Feuer&Flamme: Wachsbrand an der Reagenzglasmündung

Versuch aus der Reihe Feuer und Flamme:
Erhitzen von Wachs im Reagenzglas und Entflammen des Gase an der Mündung |  |
|
 A14d1 A14d1
Experiment
Experiment-Video
| Feuer&Flamme: Brennen auch bei Holz, Papier etc. nur die Gase?

Brennbare Stoffe werden im Reagenzglas erhitzt und es wird versucht, die entstehenden Dämpfe anzuzünden. |  |
|
 A14e A14e
Experiment
Experiment-Video
| Feuer&Flamme: Der Docht

Versuch aus der Reihe Feuer und Flamme:
Der Docht wird angezündet, in Kristallviolettlösung und in Peroleum gehalten |  |
|
 A14f A14f
Experiment
Experiment-Video
| Feuer&Flamme: Löschen von Benzinbränden

Versuch aus der Reihe Feuer und Flamme:
Es wird versucht, Leichtbenzin und Paraffin mit Wasser zu löschen |  |
|
 A14f1 A14f1
Experiment
| Feuer&Flamme: Kupferspirale

Durch die Masse des kalten Kupferdrahtes soll das Wachs unter die Entflammtemperatur gebracht werden. | 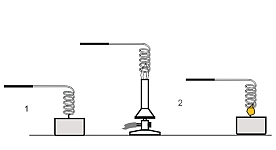 |
|
 A14f2 A14f2
Experiment
| Feuer&Flamme: Wir konstruieren einen Feuerlöscher

Wir bauen eine Apparatur, die auf Knopfdruck Wasser spritzt. |  |
|
 A14g A14g
Experiment
Experiment-Video
| Feuer&Flamme: Entflammen verschiedener Benzinsorten

Versuch aus der Reihe Feuer und Flamme:
Flüssigkeiten mit unterschiedlichen Siedepunkten: Leichtbenzin (40-60°C), Ethanol (78°C) und Petroleum (180-200°C) werden angezündet. |  |
|
 A14g1 A14g1
Experiment
Experiment-Video
| Feuer&Flamme: Entflammen von Brennergas

Es wird versucht, das aus dem Gasbrenner strömende Gas zu entzünden. |  |
|
 A14g2 A14g2
Experiment
Experiment-Video
| Feuer&Flamme: Warum sind Flammen fast immer gelb?

1) Es wird ein Magnesiastäbchen oder ein kaltes Reagenzglas über eine Kerzenflamme gehalten.
2) Es wird Ruß (Kohlestaub) in eine nichtleuchtende Flamme gestreut.
|  |
|
 A14h A14h
Experiment
Experiment-Video
| Feuer&Flamme: Die Rolle des brandfördernden Stoffes

Zwei Teelichte werden unter unterschiedlich großen Bechergläsern gleichzeitig entzündet, um die Rolle der Umgebungsluft zu studieren |  |
|
 A14h1 A14h1
Experiment
| Exkurs: Pneumatisches Auffangen von Gasen

In einen mit Wasser gefüllten Standzylinder wird ein Gas eingeleitet | 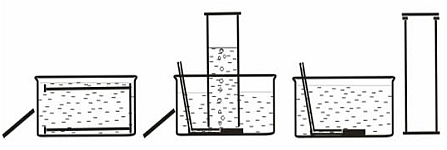 |
|
 A14h2 A14h2
Experiment
Experiment-Video
| Feuer&Flamme: Verbrennungen in reinem Sauerstoff

Eine Kerze, glühende Eisenwolle und glühende und brennende Holzwolle werden in reinen Sauerstoff gehalten. |  |
|
 A14h3 A14h3
Experiment
| Feuer&Flamme: Wird Eisen beim Verbrennen leichter?

Eisenwolle wird an einer Balkenwaage verbrannt und dabei gewogen | 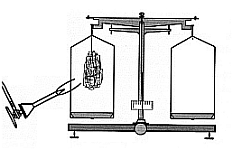 |
|
 A14h4 A14h4
Experiment
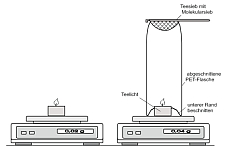
| Feuer&Flamme: Wird eine Kerze beim Verbrennen leichter?

Eine Kerze (Teelicht) brennt auf der Waage ab.
a) ohne Maßnahmen b)Die Verbrennungsprodukte werden aufgefangen und mit gewogen
|  |
|
 A14i A14i
Experiment
Experiment-Video
| Feuer&Flamme: Knallt wie der 'steyrische Hochzeitsböller'

Ein Ethin/Sauerstoff-Gemisch wird optimal eingestellt und dann in Seifenblasen gezündet |  |
|
 A14j A14j
Experiment
Selbstbau
Experiment-Video
| Feuer&Flamme: Die Erdgasmamba

Erdgas wird durch eine Seifenlösung geleitet. Die aneinanderklebenden Bläschen vermitteln den Eindruck einer Schlange. Diese kann angezündet werden |  |
|
 A14k A14k
Experiment
Experiment-Video
| Feuer&Flamme: Kann man Papier mit einer Kerze entflammen?

Versuch aus der Reihe Feuer und Flamme:
Ein Teeleicht wird unter einem Papiertrichter gestellt: Er geht in Flammen auf.
Beim zweiten Versuch ist der Papiertrichter mit Wasser gefüllt - Er lässt sich nun nicht mehr entflammen. |  |
|
 A14l A14l
Experiment
Experiment-Video
| Feuer&Flamme: Der Flammentod eines Gummibärchens

Versuch aus der Reihe Feuer und Flamme:
Raum abdunkeln! In einem ganz leicht schräg eingespannten Reagenzglas erhitzt man rund 10 g Kaliumchlorat bis zum Schmelzen. Unmittelbar danach gibt man das Gummibärchen hinzu, welches sofort unter heftigem Tanzen mit einer bläulichen Farbe verbrennt. Begleitet wird der Vorgang von einem kräftigen Brummen und Zischen. |  |
|
 A14l1 A14l1
Experiment
Experiment-Video
| Feuer&Flamme: Wunderkerzen unter Wasser

Wunderkerzen enthalten einen brennbaren und brandfördernden Stoff. Bindet man sie zusammen, so kühlen sie nicht unter die Entflammtemperatur ab, wie eine einzelne |  |
|
 A14m A14m
Experiment
Experiment-Video
| Feuer&Flamme: Der Petroleumzerstäuber

Versuch aus der Reihe Feuer und Flamme:
In Versuch 2f brannte Petroleum eigentlich nur, wenn das Streichholz in der Nähe war. Nun sprühen wir das Petroleum mit einem Zerstäuber in die Brennerflamme: Es entsteht eine Stichflamme. |  |
|
 A14n A14n
Experiment
Selbstbau
Experiment-Video
| Feuer&Flamme: Zündung im Automotor

Versuch aus der Reihe Feuer und Flamme:
In einem Automotor wird der brennbare Stoff gasförmig gemacht und mit Luft vermischt. Dies geschieht im Vergaser. Die Zündung erfolgt im Modellmotor. |  |
|
 A14o A14o
Experiment
Experiment-Video
| Feuer&Flamme: Brandfrage für Feuerexperten

Versuch aus der Reihe Feuer und Flamme:
Zwei Kerzen werden in unterschiedlicher Höhe in einem Gurkenglas aufgebaut und entflammt. Dann wird das Glas mit dem Deckel verschlossen.... Welche Kerze geht zuerst aus? |  |
|
 A14p A14p
Experiment
Experiment-Video
| Feuer&Flamme: Feuerspucken

Versuch aus der Reihe Feuer und Flamme:
Auch feste Stoffe haben eine große OBerfläche, wenn sie kleingewnug sind: Bärlappsporen |  |
|
 A14q A14q
Experiment
Experiment-Video
| Feuer&Flamme: Feuer-Tornado

Versuch aus der Reihe Feuer und Flamme:
Durch Drehung des Metallgitters wird der Kamineffekt verstärkt: Es entsteht ein Wirbelfeuer!
(Leider sieht die Kamera die Lichtreflexionen am Metallnetz deutlicher als die Augen!) |  |
|
 A14r A14r
Experiment
Selbstbau
Experiment-Video
| Feuer&Flamme: Feuer im Schlauch (Spirale)

Versuch aus der Reihe Feuer und Flamme:
Benzindampf sinkt im Schlauch herunter, bis er von einem Teelicht angezündet wird..... |  |
|
A14s
Experiment
Experiment-Video
| Feuer&Flamme: Das pulsierende Herz

Versuch aus der Reihe Feuer und Flamme:
Ein Platinkatalysatorherz glüht im Methanoldampf pulsierend auf. |  |
|
B01
Experiment
| Reagenzien für die qualitative anorganische Analyse

Anleitung zur Herstellunge der benötigten Reagenzien für die qualitative anorganische Analyse | |
|
B02
Experiment
| Qualitative Analyse: Anionen

Anionen
Eine Lösung des entsprechenden Ions wird mit einem möglichst spezifischen Reagenz behandelt und anhand einer charakteristischen Reaktion (Verfärbung oder Niederschlag) identifiziert. | |
|
B03
Experiment
| Qualitative Analyse: Kationen

Kationen
Eine Lösung des entsprechenden Ions wird mit einem möglichst spezifischen Reagenz behandelt und anhand einer charakteristischen Reaktion (Verfärbung oder Niederschlag) identifiziert. | |
|
 B04 B04
Experiment
| Flammenfärbung

Die Salze einiger Metalle werden mit Hilfe eines Magnesiastäbchens in den Flammensaum gehalten und die entstehende Flammenfärbung direkt bzw. durch ein Spektroskop beobachtet. | |
|
 B04a B04a
Experiment
| Flammenfärbung mit Ultraschallzerstäuber

Die Lösungen einiger Metallsalze werden mit Hilfe eines Ultraschallzerstäubers sehr fein in die Luftansaugzone des Bunsenbrenners gesprüht und die entstehende Flammenfärbung direkt bzw. durch ein Spektroskop beobachtet. |  |
|
B05
Experiment
| Trennungsgang : Beispiel: Erdalkali - Gruppe

Zur Auftrennung der drei Erdalkaliionen Ca2+, Sr2+ und Ba2+ bedient man sich ihres unterschiedlichen Verhaltens gegenüber Chromat-, Dichromat- bzw. Sulfat-Lösungen. | |
|
 C02 C02
Experiment
| Titrationsübung

Herstellen und Überprüfen einer Natronlauge mit der Konzentration c = 0,1 mol/L | |
|
 C03 C03
Experiment
| Fällungstitration: Bestimmung des Chloridgehaltes einer Wasserprobe

Chlorid- Ionen werden mit Silbernitrat ausgefällt. Es bildet sich ein weißer schwerlöslicher Niederschlag aus Silberchlorid - Als Indikator dient Kaliumchromat. Die Fällung des Silberchromat beginnt erst, wenn das Chlorid schon gefällt ist. Bromid und Iodid- Ionen werden bei der Bestimmung mit erfaßt. | |
|
 C04 C04
Experiment
| Manganometrie: Bestimmung des Kaliumpermanganat-(KMnO4)-Verbrauchs einer Wasserprobe

Mit Hilfe des Kaliumpermanganat-(KMnO4)-Verbrauchs eines natürlichen Gewässers läßt sich auch dessen Verschmutzungsgrad bestimmen. Dabei werden die organischen Verunreinigungen oxidiert. Der Verbrauch an Oxidationsmittel (KMnO4) läßt auf den Grad der Verschmutzung schließen | |
|
 C05 C05
Experiment
| Iodometrie: Bestimmung des Sauerstoffgehaltes einer Wasserprobe

Im alkalischen Bereich reagiert Mangan(II) - chlorid mit dem gelösten Sauerstoff zu gemischten Hydroxiden, die im sauren quantitativ zu Mangan (III) -Ionen reagieren. Diese werden mit Iodid - Ionen reduziert und entstandenes Iod mit Natriumthiosulfat bestimmt. | |
|
 C06 C06
Experiment
| Komplexometrie: Bestimmung des Calcium- und Magnesiumionengehaltes einer Wasserprobe

Viele Metalle, so die Erdalkali - Ionen bilden mit Ethylen - Diammin - Tetra - Essigäure stabile Komplexe. Der Äquivalenzpunkt wird durch einen Indikator, der selbst einen (schwächeren) Komplex bildet, angezeigt. | |
|
 C10 C10
Experiment
| Quantitative Analyse von Silberoxid

In einem einfachen Versuch lässt sich durch Erwärmen im Reagenzglas eine Thermolyse von Silberoxid durchführen. | |
|
 C11 C11
Experiment
| Quantitative Synthese: Welche Formel hat Kupferoxid?

Kupfer reagiert mit einem Überschuss an Schwefel im Tiegel und die Massen werden bestimmt. | |
|
 D01 D01
Experiment
Selbstbau
| Aufbau einfacher elektrischer Schaltungen: 'Leitfähigkeit' einer Glühbirne

In dieser Übung wird eine elektrische Schaltung zur Messung von Spannung und Stromstärke bei dem Betrieb eines Lämpchens aufgebaut und betrieben. |  |
|
 D02 D02
Experiment
Teachers Helper
AK Multiadapter
Multiadapter TH
Selbstbau
All-Chem-Misst
LowCost-Leitfähigkeit
Experiment-Video
| Messung der elektrischen Leitfähigkeit unterschiedlicher Lösungen

"Zur Messung der elektrischen Leitfähigkeit von Lösungen wird das Lämpchen später gegen einen Leitfähigkeitsprüfer ausgetauscht und die Wechselspannung auf einen festen Wert eingestellt. Da in Lösungen der Stromtransport ausschließlich durch Ionen geschieht, hängt die elektrische Leitfähigkeit in erster Linie von drei Faktoren ab. 1. der Konzentration, 2. der Ladungsgröße und 3. der Beweglichkeit der Ionen. Es werden unterschiedlichste Lösungen untersucht und Aussagen über deren Ionen gemacht. Der Rechner dient nicht zum Verwalten der Daten sondern als Großanzeige. Da es sich um Wechselspannung handelt, kann der Versuch nicht mit dem ALL-CHEM-MISST durchgeführt werden." |  |
|
D03
Experiment
AK Analytik 32.NET
All-Chem-Misst
| Bestimmung der Äquivalentleitfähigkeit von Säuren, Laugen und Salzlösungen

Es wird eine Verdünnungsreihe der jeweiligen Salzlösung hergestellt und von dieser die elektrische Leitfähigkeit gemessen |  |
|
D04
Experiment
AK Analytik 32.NET
All-Chem-Misst
| Best. der Äquivalentleitfähigkeit und der Dissoziationskonstanten von Essigsäure

Die Versuchsdurchführung verläuft völlig analog zu Arbeitsblatt D03. Auf diesem ist auch schon eine Spalte für die Versuchsergebnisse dieses Arbeitsblattes vorgesehen. Die Auswertung geschieht hier allerdings unter Einbeziehung des Massen - Wirkungs - Gesetzes. |  |
|
D05
Experiment
AK Analytik 32.NET
All-Chem-Misst
| Best. der Äquivalentleitf. und der Dissoziationskonstanten von Essigs. (Variante)

Essigsäure ist ein schwacher Elektrolyt. Die Leitfähigkeit bei sehr kleinen unterschiedlichen Verdünnungen wird gemessen und graphisch die Dissoziationskonstante bestimmt. |  |
|
 D06 D06
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Leitfähigkeit
| Leitfähigkeit bei unterschiedlichen Verdünnungen von Essigsäure

Es wird eine Verdünnungsreihe von Essigsäure hergestellt und von dieser die elektrische Leitfähigkeit gemessen. |  |
|
 D07 D07
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Leitfähigkeit
| Konduktom. Titration von Bariumhydroxid - Lsg. mit Salzsäure

Die Reaktion muss wie eine normale Neutralisation betrachtet werden.
 Low-Cost-Titration möglich analog zu Experiment D10l Low-Cost-Titration möglich analog zu Experiment D10l |  |
|
 D08 D08
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| Bestimmung und Beurteilung der Leitfähigkeit von Wasserproben

Der Stromtransport in Lösungen geschieht ausschließlich durch Ionen. Mit der Messung der elektrischen Leitfähigkeit bei Wässern werden alle dissoziierten Stoffe erfasst. Sie ist ein sogenannter Summenparameter und gibt Aufschluss über den Elektrolytgehalt. |  |
|
 D09 D09
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Leitfähigkeit
| Konduktometrische Titration von Chlorid - Lösung mit Silbernitrat - Lösung

Im vorliegenden Fall handelt es sich um eine Fällungsreaktion. Die Chlorid - Ionen werden durch Zugabe von Silbernitratlösung als Silberchlorid ausgefällt. Die Änderung der elektrischen Leitfähigkeit wird gemessen.
 Low-Cost-Titration möglich analog zu Experiment D10l Low-Cost-Titration möglich analog zu Experiment D10l |  |
|
 D10 D10
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Leitfähigkeit
| Konduktometrische Titration von Salzsäure mit Natronlauge

Da sich bei der Neutralisation die Leitfähigkeit ändert, kann man die Titration auch konduktometrisch verfolgen. Die Qualität der Endpunkterkennung soll anhand der Neutralisation von Reaktionspartnern unterschiedlicher Konzentration beurteilt werden. |  |
|
 D10l D10l
Experiment
LowCost-Leitfähigkeit
| LowCost: Konduktometrische Titration von Salzsäure mit Natronlauge

Es soll die Änderung der Stromstärke bei der Titration von Salzsäure (c= 0,1 mol/L) mit Natronlauge (c= 0,1 mol/L) mit Hilfe eines Fernost-Multimeters und eines Computers verfolgt werden. Dabei wird die Lauge langsam zugetropft und der Messwert durch Druck auf die Leertaste (im Intervall von 0,5 mL) vom Computer registriert |  |
|
 D11 D11
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Leitfähigkeit
| Konduktometrische Titration von Essigsäure mit Natronlauge

Da sich bei der Neutralisation die Leitfähigkeit ändert, kann man die Titration auch konduktometrisch verfolgen. Die Qualität der Endpunkterkennung soll anhand der Neutralisation von Reaktionspartnern unterschiedlicher Konzentration beurteilt werden. |  |
|
 D12 D12
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Leitfähigkeit
| Konduktom. Titration eines Gemisches von Salz- /Essigsäure mit Natronlauge

Da sich bei der Neutralisation die Leitfähigkeit ändert, kann man auch die Titration eines Gemisches aus starker und schwacher Säure konduktometrisch verfolgen. |  |
|
 D13 D13
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Leitfähigkeit
| Konduktometrische Titration von Phosphorsäure mit Natronlauge

Da sich bei der Neutralisation die Leitfähigkeit ändert, kann man die Titration auch konduktometrisch verfolgen. Die Phosphorsäure mit ihren unterschiedlichen Protolysestufen eignet sich recht gut zum Studium des unterschiedlichen Verhaltens der Ionen. |  |
|
 D14 D14
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Leitfähigkeit
| Konduktometrische Titration von Ammoniak - Lösung mit Essigsäure

Hier soll die Änderung der Leitfähigkeit bei der Titration zweier schwacher Elektrolyte verfolgt werden. |  |
|
 D15 D15
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Leitfähigkeit
| Konduktom. Titration von Bariumhydroxid - Lsg. mit Schwefelsäure

Neben der normalen Neutralisation muss im Fall der Schwefelsäure auch die Ausfällung der Barium- bzw. Sulfat - Ionen betrachtet werden.
 Low-Cost-Titration möglich analog zu Experiment D10l Low-Cost-Titration möglich analog zu Experiment D10l |  |
|
 D16 D16
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Leitfähigkeit
| Umsetzung von Magnesium mit Salzsäure

Bei der Reaktion von Magnesium mit Salzsäure werden Oxonium - Ionen verbraucht. Neben der Messung des pH - Wertes und des Volumens des entstehenden Wasserstoffs bietet sich eine Verfolgung der Reaktion über eine Leitfähigkeitsmessung an. |  |
|
 D17 D17
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Leitfähigkeit
| Verseifung von Ethansäureethylester

Bei der alkalischen Verseifung von Ethansäureethylester werden Hydroxid - Ionen durch Acetat - Ionen ersetzt. Daher kann die Reaktion mit Hilfe der Leitfähigkeitsmessung verfolgt werden. |  |
|
 D18 D18
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Leitfähigkeit
| Harnstoffspaltung durch Urease

Bei der Spaltung von Harnstoff durch Urease entstehen Kohlenstoffdioxid und Ammoniak, wobei insbesondere letzteres mit Wasser leicht zu Ammonium - und Hydroxid - Ionen reagiert. Daher bietet sich eine Verfolgung der Reaktion über eine Leitfähigkeitsmessung an.
 Low-Cost-Messung möglich analog zu Experiment D10l Low-Cost-Messung möglich analog zu Experiment D10l |  |
|
 D19 D19
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| Hydrolyse von 2-Chlor-2-Methylpropan

Die Hydrolyse von tert. Butylchlorid in wässriger Lösung kann mit Hilfe der Leitfähigkeitsmessung verfolgt werden, da dabei Oxonium - und Chlorid - Ionen entstehen. Der Versuch wird über einen gewissen Zeitraum gemessen und die Daten unter reaktionskinetischen Gesichtspunkten ausgewertet |  |
|
 D20 D20
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| Temperaturabhängigkeit der Hydrolyse von 2-Chlor-2-Methylpropan

Die Hydrolyse von tert.-Butylchlorid in wässriger Lösung kann mit Hilfe der Leitfähigkeitsmessung verfolgt werden, da dabei Hydroxonium - und Chlorid - Ionen entstehen. Der Versuch wird mehrfach, wie Versuch D19, nur bei verschiedenen Temperaturen durchgeführt und die Daten unter reaktionskinetischen und energetischen Gesichtspunkten ausgewertet. | |
|
 D21 D21
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| Lösungsmittelabhängigkeit der Hydrolyse von 2-Chlor-2-Methylpropan

Die Hydrolyse von tert.- Butylchlorid in wässriger Lösung kann mit Hilfe der Leitfähigkeitsmessung verfolgt werden, da dabei Oxonium- und Chlorid- Ionen entstehen. Der Versuch wird mehrfach, wie Versuch D19, mit unterschiedlichen Lösungsmittelgemischen durchgeführt und die Daten unter reaktionskinetischen Gesichtspunkten ausgewertet, um Aufschluss über den Reaktions-mechanismus zu erhalten | |
|
 D22 D22
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| MWG: I.Verseifung und II Veresterung von Methansäure

In zwei separaten Ansätzen wird die Verseifung von Ameisensäuremethylester bzw. die Veresterung von Ameisensäure mit Methanol mit Hilfe der Leitfähigkeitsmessung verfolgt. |  |
|
 D23 D23
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| Quantitative Bestimmung des Chlorid - Gehaltes in Blut - Serum

Der Chlorid - Gehalt im Serum wird durch Titration nach MOHR bestimmt. Dabei wird Silbernitrat aus einer Bürette in ein mit Kaliumchromat (Indikator) versetztes Serumfiltrat getropft. Solange Chlorid - Ionen im Serum vorhanden sind, fällt ein Niederschlag von Silberchlorid aus. Gleichzeitig reagieren die Chromat - Ionen mit den Silberionen zu rotbraunem Silberchromat, das jedoch erst bei einer sehr kleinen Chlorid - Konzentration ausfällt, da es leichter löslich ist als Silberchlorid. Bei der Titration wird die Änderung der Leitfähigkeit verfolgt.
 Low-Cost-Titration möglich analog zu Experiment D10l Low-Cost-Titration möglich analog zu Experiment D10l |  |
|
 E01 E01
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
All-Chem-Misst
LowCost-Potential
| Zellspannung und Konzentration bei Silber- und Kupferlösungen

Es wird eine Konzentrationskette erstellt, wobei in einer Halbzelle, die das Bezugs - Element darstellt, die Konzentration an Ionen konstant bleibt, und in der anderen die Ag+- bzw. Cu2+- Konzentration nacheinander erniedrigt wird. |  |
|
 E02 E02
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Potential
| Bestimmung der Konzentration von Silberionen

Aus der Tatsache, daß die Silberionenkonzentration durch unterschiedliche Löslichkeitsprodukte und Komplexdissoziationskonstanten kontrolliert wird, läßt sich eine sehr schöne Versuchsreihe konzipieren. |  |
|
 E03 E03
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| Laden und Entladen eines Bleiakkus

Die Spannungsverhältnisse beim Laden bzw. Entladen eines Bleiakkus, der meist benutzten wieder aufladbaren Batterie soll untersucht werden. |  |
|
 E03a E03a
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
Selbstbau
All-Chem-Misst
| Die Zink-Iod-Zelle (Der didaktische Wunderakku)

Hier wird augenfällig mit einem simplen Aufbau demonstriert, wie elektrische Energie chemisch gespeichert und wieder abgerufen kann. Das Experiment macht erfahrungsgemäß sehr viel Freude. |  |
|
 E04 E04
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Potential
| Bestimmung des Chlorid-, Bromid- und Iodid- Gehaltes einer Lösung

Die Halogenidlösung wird mit Silbernitratlösung titriert. Die Titration wird dabei potentiometrisch verfolgt. Es kommt zur Bildung schwerlöslicher Silberhalogenide, die mit ihrem Löslichkeitsprodukt die Silberionenkonzentration kontrollieren. |  |
|
 E05 E05
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Potential
| Bestimmung des Gehaltes einer Iod- Lösung mit Natriunthiosulfat - Lösung

Die Probe der Iod-lösung wird mit Natrimthiosulfatlösung (c= 0,1 mol/L) titriert und potentiometrisch verfolgt. Es kommt zu einem Reaktionsgleichgewicht, dessen Gleichgewichtskonstante es zu berechnen gilt. |  |
|
 E06 E06
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Potential
| Verfolgung einer oszillierenden Reaktion

Oszillierende Reaktionen lassen sich nicht nur als faszinierende Farbenspiele beobachten. Bei der Belousov - Zabotinsky- Reaktion lässt sich auch die Potentialänderung mit dem "chemischen Oszilloskop" gut verfolgen. |  |
|
 E07a E07a
Experiment
Teachers Helper
AK Multiadapter
Multiadapter TH
All-Chem-Misst ohne Rechner
LowCost-Potential
Experiment-Video
| Elektrochemische Spannugsquelle: Cu/Zn-Büroklammerbatterie

Es ist immer wieder verblüffend, wie der "Strom aus der kleinen Büroklammer" gewonnen wird.
Die Spannung kann gemessen werden - auch der Motor dreht sich.
| |
|
 E07b E07b
Experiment
Teachers Helper
AK Multiadapter
Multiadapter TH
All-Chem-Misst ohne Rechner
LowCost-Potential
Experiment-Video
| Elektrochemische Spannugsquelle: Cu/Zn-Zitronenbatterie

Es ist immer wieder verblüffend, wie vermeintlicherweise der "Strom aus der Zitrone" gewonnen wird.
Die Spannung kann gemessen werden - auch der Motor dreht sich.
| |
|
 E07c E07c
Experiment
Teachers Helper
AK Multiadapter
Multiadapter TH
All-Chem-Misst ohne Rechner
LowCost-Potential
Experiment-Video
| Elektrochemische Spannugsquelle: Cu/Zn- Äpfel- Birnen- Kartoffelbatterie

Man kann auf die gleiche Weise (siehe Zitronenbatterie AB E07b) auch andere Obstsorten einsetzen. Es muss keine Zitronensäure vorhanden sein. Je nach Flüssigkeitsgehalt und Reifegrad erhält man leicht unterschiedliche Ergebnisse. | |
|
 E07d E07d
Experiment
Teachers Helper
AK Multiadapter
Multiadapter TH
All-Chem-Misst ohne Rechner
LowCost-Potential
Experiment-Video
| Elektrochemische Spannugsquelle: Cu/Zn- Leitungswaaser -Batterie

Es ist immer wieder verblüffend, wie vermeintlicherweise aus "Leitungswasser" Strom gewonnen wird.
Die Spannung kann gemessen werden - auch der Motor dreht sich.
| |
|
 E08 E08
Experiment
Teachers Helper
AK Multiadapter
Multiadapter TH
All-Chem-Misst ohne Rechner
LowCost-Potential
Experiment-Video
| Elektrochemische Spannugsquelle: Mg/I2-Batterie

Hier werden unterschiedliche elektrochemische Zellen, die sich für den Unterricht eignen, vorgestellt.
Dabei wechseln Elektrodenmaterial und Elektrolyt.
| |
|
 E09a E09a
Experiment
Teachers Helper
AK Multiadapter
Multiadapter TH
All-Chem-Misst ohne Rechner
LowCost-Potential
Experiment-Video
| Elektrochemische Spannugsquelle: Mg/O2- Salzwasser- Batterie

Die "Magnesium- Luft- Batterie" - einige Tropfen Salzwasser (in Meerwasserkonzentration) als Elektrolyt genü-gen. Magnesiumsalze gibt es in den Meeren genug. | |
|
 E09b E09b
Experiment
All-Chem-Misst ohne Rechner
LowCost-Potential
Experiment-Video
| Elektrochemische Spannugsquelle: Mg/O2- Salzwasser- Auto

Die "Magnesium- Luft- Batterie" - einige Tropfen Salzwasser (in Meerwasserkonzentration) als Elektrolyt gengen und das Modellauto fährt. Magnesiumsalze gibt es in den Meeren genug. | |
|
 E10 E10
Experiment
Teachers Helper
AK Multiadapter
Multiadapter TH
All-Chem-Misst ohne Rechner
LowCost-Potential
Experiment-Video
| Elektrochemische Spannugsquelle: Al/O2-'RedBull' - Batterie

Als Aluminium-Material bieten sich Getränkedosen oder Teelichter an (Achtung: die abgebildete Cola-Dose ist aus Weißblech! Als Elektrolyt kann Salzwasser dienen. | |
|
 F01 F01
Experiment
AK Analytik 11
AK Analytik 32.NET
Theorie
All-Chem-Misst
LowCost-pH
| Allgemeine Anleitung zur Kalibrierung von pH-Messgeräten (Ur-ALL-CHEM-MISST)

Hinweise zur Kalibrierung unterschiedlicher pH-Messgeräte (insbesondere All-Chem-Misst) |  |
|
 F02 F02
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-pH
| pH-Wert-Messungen in Lösungen (mit Kalibrierung)

Mit dem ALL-CHEM-MISST II ist es besonders einfach, pH-Werte zu messen. Die Werte können auf sehr großen Anzeige oder einem Beamer dargestellt werden. Natürlich ist auch die Messwertübertragung zum Rechner möglich.
Besonderheit: Die lästige, aber bei pH-Elektroden notwendige Kalibrierung ist ganz einfach, weil jeder Schritt auf dem Touchscreen vorgegeben wird. |  |
|
 F03 F03
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-pH
| Titration von Salzsäure mit Natronlauge

Da sich bei der Neutralisation der pH- Wert ändert, kann man die Titration potentiometrisch verfolgen. |  |
|
 F03l F03l
Experiment
AK Analytik 11
AK Analytik 32.NET
LowCost und Medizin-Technik
All-Chem-Misst
LowCost-pH
| Titration von Salzsäure mit Natronlauge mit 'easy pH'

Da sich bei der Neutralisation der pH- Wert ändert, kann man die Titration per LowCost- Potenziometrie verfolgt werden. |  |
|
 F04 F04
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-pH
| Titration von Essigsäure mit Natronlauge (mit pKs-Wert-Bestimmung)

Essigsäure wird mit Natronlauge titriert. Durch Ermittlung des Äquivalenzpunktes läßt sich der Gehalt der Säure berechnen, durch Ermittlung des Halbäquivalenzpunktes der entsprechende pKs- Wert. |  |
|
 F04a F04a
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-pH
| Titration von Speiseessig mit Natronlauge

Speiseessig wird mit Natronlauge titriert. Er muss mindestens 5% Essigsäure enthalten. |  |
|
 F05 F05
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-pH
| Titration eines Gemisches von Salz-/Essigsäure mit Natronlauge

Das Gemisch aus Salz- und Essigsäure wird mit Natronlauge titriert. Durch Ermittlung der Äquivalenzpunkte lässt sich der Gehalt der beiden Säuren berechnen. |  |
|
 F06 F06
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-pH
| Titration von Phosphorsäure mit Natronlauge

Phosphorsäure wird mit Natronlauge titriert. Durch Ermittlung eines Äquivalenzpunktes lässt sich der Gehalt der Säure berechnen, durch Ermittlung der Halbäquivalenzpunkte die pKs- Werte. |  |
|
 F07 F07
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-pH
| Titration von Malonsäure mit Natronlauge

Malonsäure als Vertreter einer dreibasigen Säure werden hier stellvertretend vorgestellt. |  |
|
 F07a F07a
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-pH
| Titration von Histidindihydrochlorid mit Natronlauge

Histidin als Vetreter einer dreibasigen Säure wird hier stellvertretend vorgestellt. |  |
|
 F08 F08
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-pH
| Titration von Glycin mit Natronlauge und Salzsäure

Die Aminosäure Glycin wird mit Natronlauge titriert. Durch Ermittlung des Äquivalenzpunktes lässt sich der Gehalt der Säure berechnen, durch Ermittlung des Halbäquivalenzpunktes der entsprechende pKs- Wert II. Durch eine weitere Titration mit Salzsäure kann auch der pKs-Wert I ermittelt werden. |  |
|
 F09 F09
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-pH
| Titration von Ammoniak-Lösung mit Essigsäure

Essigsäure wird mit Ammoniak - Lösung titriert. Es handelt sich hierbei um die Reaktion einer schwachen Säure mit einer schwachen Base. Durch Ermittlung des Äquivalenzpunktes lässt sich der Gehalt der Säure berechnen, durch Ermittlung des Halbäquivalenzpunktes der entsprechende pKs- Wert. |  |
|
 F10 F10
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-pH
| Titration von Mineralwässern und COLA-Getränken

Zum Nachweis von Kohlensäure werden Mineralwasser zum einen direkt, zum anderen nach einem etwa 15 minütigem Verkochen mit Natronlauge titriert und dabei der pH-Wert gemessen. |  |
|
 F10a F10a
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-pH
| Titration von COLA-Getränken

Zum Nachweis von Kohlensäure bzw. Phosphorsäure werden COLA- Getränke zum einen direkt, zum anderen nach einem etwa 15 minütigem Verkochen mit Natronlauge titriert und dabei der pH-Wert gemessen. |  |
|
 F11 F11
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-pH
| Bestimmung von Ameisensäure in einem Kalklöser

Im Handel erhältlicher Kalklöser wird mit Natronlauge titriert. Der Gehalt wird bestimmt und die vorhandene Säure aufgrund des pKs-Wertes als Ameisensäure identifiziert. |  |
|
 F12 F12
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-pH
| Hydrolyse von 2- Chlor -2- Methylpropan

Die Hydrolyse von tert. Butylchlorid in wässriger Lösung kann mit Hilfe der pH - Wert - Messung verfolgt werden, da dabei Oxoniumionen entstehen. Der Versuch wird über einen Zeitraum vermessen und die Daten unter reaktionskinetischen Gesichtspunkten ausgewertet. |  |
|
G00
Experiment
LowCost-Temperatur
Experiment-Video
| Temperatur(en) einer Kerzenflamme: Wer misst, misst Mist!

Ein (digitales) Thermometer zeigt mit einem normalen Labor-Edelstahl-Temperaturfühler die Temperatur einer Kerzenflamme mit etwa 550°C an; mit einem Drahtfühler werden dagen knapp 1000°C gemessen.
|  |
|
 G01 G01
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Temperatur
| Bestimmung des Wasserwertes eines Kalorimeters

Die Temperaturänderung beim Zusammengeben zweier Wassermengen mit unterschiedlicher Temperatur wird gemessen und so der Wasserwert, ein Eichwert für das Kalorimeter ermittelt. |  |
|
 G02 G02
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Temperatur
| Bestimmung der Lösungswärme von Salzen (Kupfersulfat, Kaliumchlorid)

Eine Salzportion wird im Kalorimeter gelöst und die dabei entstehende Wärmemenge berechnet. Nimmt man wasserfreies Kupfersulfat und blaues Kupfersulfat, so läßt sich nach dem Satz von Hess die Hydratationswärme berechnen. |  |
|
 G03 G03
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Temperatur
| Bestimmung derMolare und spezifische Schmelzwärme von Eis

Die Temperaturerniedrigung beim Schmelzen von Eis wird im Kalorimeter gemessen und die zugehörige Enthalpieänderung berechnet. |  |
|
 G04 G04
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Temperatur
| Bestimmung der Mischungswärme von Wasser - Methanol

Die Temperaturerhöhung bei der Mischung von Wasser mit Methanol wird im Kalorimeter gemessen und die zugehörige Enthalpieänderung berechnet. Da die Dauer des Versuchs recht kurz ist, kann er mit unterschiedlichen Mischungsverhältnissen wiederholt werden. |  |
|
 G05 G05
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Temperatur
| Schmelzen / Abkühlen von Natriumthiosulfat

Im folgenden Versuch soll untersucht werden wie sich die Temperatur beim Erhitzen und Abkühlen von festem Natriumthiosulfat bzw. dessen Schmelze ändern. |  |
|
 G06 G06
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Temperatur
| Bestimmung der Neutralisationsenthalpie

Da die Neutralisation eine exotherme Reaktion ist, läßt sich die Neutralisationswärme auch bei Reaktionen unterschiedlich starker bzw. konzentrierter Säuren bestimmen. |  |
|
 G07 G07
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Temperatur
| Bestimmung der Bildungswärme von Eisensulfid

Eisen reagiert mit Schwefel exotherm. Die Bildungsenthalpie läßt sich in einem einfachen Kalorimeter bestimmen. |  |
|
 G08 G08
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Temperatur
| Bestimmung der Reaktionsenthalpie einer Redoxreaktion (Kupferionen - Zink)

Die Wärmemenge, die entsteht, wenn man einen Überschuß von Zink auf eine Kupfersalzlösung einwirken läßt, wird gemessen. |  |
|
 G09 G09
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
LowCost und Medizin-Technik
All-Chem-Misst
LowCost-Temperatur
| Verbrennungswärmen einiger Alkohole

In einem einfachen Becherglaskalorimeter wird soviel Alkohol verbrannt, bis die Wassertemperatur um einen gewissen Betrag gestiegen ist. Auf gleiche Weise wird das Kalorimeter mit einem Alkohol bekannter Verbrennungsenthalpie geeicht. Der Versuch läßt sich auch ohne Computer durchführen, dieser dient hier zur Großanzeige der Temperatur. |  |
|
 G10 G10
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Temperatur
| Bestimmung des Heizwertes von brennbaren Lebensmitteln

Die Bestimmung des Heizwertes von brennbaren Lebensmitteln z.B. Popcorn. |  |
|
 G11 G11
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Temperatur
| Bestimmung der Reaktionsenthalpie einer Redoxreaktion (Kupferionen - Eisen)

Die Wärmemenge, die entsteht, wenn man einen Überschuß von Eisen auf eine Kupfersalzlösung einwirken läßt, wird gemessen. |  |
|
 G12 G12
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Temperatur
| Bestimmung Kondensationswärme von Wasser

Wasserdampf wird in das Kalorimeter geleitet, die entsprechende Temperaturerhöhung gemessen und die zugehörige Enthalpieänderung berechnet. |  |
|
 G13 G13
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
LowCost und Medizin-Technik
Selbstbau
All-Chem-Misst
Experiment-Video
| Druckverflüssigung - Kühlschrank

Mit Hilfe einer angebohrten Schnellschraubzwinge wird Feuerzeuggas in einer Spritze komprimiert und wieder expandiert. Dabei wird die Temperatur gemessen. |  |
|
 G14 G14
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Temperatur
| Rektifikation bzw. Destillation von Rotwein

In einer Destillationsapparatur aus AK SÜS- Teilen, in der im zweiten Versuch ein Hempel- Rohr eingesetzt wird, das in einem dritten Versuch mit Raschig- Ringen gefüllt wird, läßt sich die Problematik der Wasser- Alkohol- Trennung durch Destillation bzw. Rektifikation sehr schön erarbeiten. Dazu wird jeweils der Temperaturverlauf gemessen. |  |
|
 G15 G15
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Temperatur
| Thermometrische Titration von Salzsäure mit Natronlauge

Da die Neutralisation eine exotherme Reaktion ist, kann man die Titration auch thermometrisch verfolgen. Die Qualität der Endpunkterkennung soll anhand der Neutralisation von Reaktionspartnern unterschiedlicher Konzentration beurteilt werden. |  |
|
 G16 G16
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
LowCost-Temperatur
| Verhalten von Wasser beim Erhitzen

Eis wird auf einem beheizbaren Magnetrührer im Becherglas erhitzt und dabei die Temperatur gemessen. |  |
|
 G17 G17
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
Experiment-Video
| Entzündungstemperatur eines Streichholzes

In einem Kolben wird die Luft solange erhitzt, bis ein Streichholz sich selbst entzündet. Wiederholung des Versuches mit Papier und Holz. |  |
|
G18
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
Experiment-Video
| Entzündungstemperaturen von Erdgas und Campinggas

Ein Eisendraht wird mit elektrischen Strom so lange zum Glühen gebracht, bis sich Erdgas bzw. Camping- oder Feuerzeuggas von selbst entzündet. | |
|
 H01a H01a
Experiment
AK Analytik 11
AK Analytik 32.NET
| Gravimetrie : Verdunstung von Ether

Ethanol und Ether verdunsten verschieden schnell.Die Massenänderung wird eine gewisse Zeit verfolgt. |  |
|
 H01b H01b
Experiment
AK Analytik 11
AK Analytik 32.NET
| Gravimetrie : Verdunstung von Ethanol

Ethanol und Ether mit gleicher Molmasse verdunsten verschieden schnell. Die Massenänderung wird eine gewisse Zeit verfolgt. |  |
|
 H01c H01c
Experiment
AK Analytik 11
AK Analytik 32.NET
| Gravimetrie : Wasseraufnahme von Schwefelsäure

Schwefelsäure nimmt Wasser aus der Luft auf. Die Massenänderung wird eine gewisse Zeit verfolgt. |  |
|
 H02 H02
Experiment
AK Analytik 11
AK Analytik 32.NET
| Reaktion von Marmor mit Salzsäure (Reaktionskinetik)

Marmor reagiert mit Salzsäure. Das dabei entweichende Kohlenstoffdioxid führt zu einem Massenverlust, der über eine bestimmte Zeit verfolgt wird. | 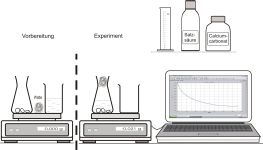 |
|
 H03 H03
Experiment
AK Analytik 11
AK Analytik 32.NET
| Katalytische Zersetzung von Wasserstoffperoxid mit Iodid-Lösung

Wasserstoffperoxid zersetzt sich unter dem Einfluß des Katalysators (Kaliumiodid- Lösung). Der dabei entweichende Sauerstoff führt zu einem Massenverlust, der über eine bestimmte Zeit verfolgt wird. |  |
|
 I01 I01
Experiment
AK Analytik 11
AK Analytik 32.NET
LowCost und Medizin-Technik
LowCost-Foto
| Zusammenhang zwischen Konzentration, Transmission und Extinktion

Eine Lösung von Kristallviolett wird mit Licht (ca. 580 nm - Grünfilter) durchstrahlt. Gesucht wird ein Zusammenhang zwischen Konzentration und Lichtschwächung. |  |
|
I02
Experiment
AK Analytik 11
AK Analytik 32.NET
| Transmissionsspektren z.B. von Bromthymolblau bei verschiedenen pH-Werten

In einem (Einstrahl)- Photometer werden nacheinander die Transmissionen von Wasser und Bromthymolblau - Lösungen bei pH=4, 7 und 10 mehr oder weniger automatisch vermessen und dabei direkt umgerechnet. | |
|
 I03 I03
Experiment
AK Analytik 11
AK Analytik 32.NET
Experiment-Video
| Extinktions- bzw. Absorptionsspektren einfach und schnell mit Diodenarrayfotometern

In einem (Einstrahl)- Photometer neuerer Bauart werden nacheinander direkt die Extinktionen von Wasser (Basislinie) und Bromthymolblau - Lösungen bei pH=4, 7 und 10 gemessen. Die Basislinie bleibt dabei im Rechner bzw. Photometer gespeichert. Dadurch wird die Handhabung recht einfach. |  |
|
 I04 I04
Experiment
AK Analytik 11
AK Analytik 32.NET
LowCost und Medizin-Technik
LowCost-Foto
| Bestimmung des Kupferanteils im Messing

Aus einer Verdünnungsreihe von Kupfer(II)-nitratlösung lässt sich eine Eichkurve erstellen mit deren Hilfe man photometrisch den Anteil des Kupfers in einer Messingprobe bestimmen kann. |  |
|
 I05 I05
Experiment
AK Analytik 11
AK Analytik 32.NET
LowCost und Medizin-Technik
LowCost-Foto
| Bestimmung von Eisen-Ionen mit Rhodanid-Lösung

Aus einer Verdünnungsreihe von Eisen(III)-nitratlösung lässt sich eine Eichkurve erstellen mit deren Hilfe man photometrisch den Anteil des Eisens in einer Probe bestimmen kann . |  |
|
 I06 I06
Experiment
AK Analytik 11
AK Analytik 32.NET
LowCost und Medizin-Technik
LowCost-Foto
| Reaktion von Kristallviolett mit Natronlauge (Reaktionskinetik)

Eine Lösung von Kristallviolett reagiert mit Natronlauge unter Bildung einer farblosen Verbindung. Die Abnahme der Farbe wird photometrisch erfasst und unter reaktionskinetischen Gesichtspunkten ausgewertet. Durch Umrechnung der Kalibrierkurve im Computer kann man auch mit sehr preiswerten Photometern direkte Konzentrationsmessungen durchführen. |  |
|
 I07 I07
Experiment
AK Analytik 11
AK Analytik 32.NET
LowCost und Medizin-Technik
LowCost-Foto
| Reaktion von Kristallv. mit Natronlauge (T- Abhängigkeit der Geschw.-konst.)

Die Farbabnahme bei der Reaktion von Kristallviolett mit Natronlauge bei unterschiedlichen Temperaturen wird photometrisch erfasst und unter reaktionskinetischen Gesichtspunkten ausgewertet. Der Versuch verläuft völlig analog zu Versuch I06. Das Ergebnis von I07 kann in die Auswertung mit aufgenommen werden. | |
|
 I08 I08
Experiment
AK Analytik 11
AK Analytik 32.NET
LowCost und Medizin-Technik
LowCost-Foto
| Anthracen-Pikrat-Gleichgewicht (MWG)

Anthracen bildet mit Pikrinsäure einen intensiv gefärbten Charge-Transfer-Komplex. Die Komplexbildungskonstante wird über die vorherige Bestimmung des Extinktionskoeffizienten für den Komplex auf photometrischem Wege ermittelt. |  |
|
 I09 I09
Experiment
AK Analytik 11
AK Analytik 32.NET
| Anthracen-Pikrat-Gleichgewicht (T- Abhängigkeit)

Bisher wurde die Temperaturabhängigkeit des Anthracen - Pikrinsäure - Gleichgewichtes meist qualitativ untersucht. Hat man jedoch den Extinktionskoeffizienten des Charge- Transferkomplexes (aus Versuch I08) so kann man das Gleichgewicht auch quantitativ untersuchen. |  |
|
 I10 I10
Experiment
AK Analytik 11
AK Analytik 32.NET
LowCost und Medizin-Technik
LowCost-Foto
| Entfärbung von Tinte mit Wasser

Eine Lösung blauer Tinte wird mit Licht (ca. 590 nm - Gelbfilter) durchstrahlt. Gesucht wird ein Zusammenhang zwischen Konzentration und Lichtschwächung. |  |
|
K01
Experiment
Theorie
| Einführung in die Chromatographie

Demonstrationsversuche zu Adsorbtion und Verteilung, Märchen, Rechenübungen und einführende Experimente zur Gaschromatographie | |
|
 K01a1 K01a1
Experiment
LowCost-GC
Experiment-Video
| Schnellversuch zur Chromatografie mit Kreide

Filzstiftfarbe wird in zwei Komponenten mit Alkohol auf Kreide aufgetrennt |  |
|
 K01a2 K01a2
Experiment
LowCost-GC
Experiment-Video
| Schnellversuch zu den Kapillarkräften

In diesem kleinen Versuch soll gezeigt werden, dass Flüssigkeit in verschieden engen Glasröhren verschieden hoch steigt. |  |
|
 K01a3 K01a3
Experiment
LowCost-GC
Experiment-Video
| Schnellversuch zu Adsorption/Desorption

Es soll untersucht werden, in wie weit Stoffe an Substanzen mit großer Oberfläche haften bzw. sich wieder davon ablösen lassen.
|  |
|
 K01a4 K01a4
Experiment
LowCost-GC
Experiment-Video
| Schnellversuch zur Verteilung

Es soll untersucht werden, in wie weit sich ein Stoff in zwei nicht miteinander mischbaren Flüssigkeiten löst. |  |
|
 K01b K01b
Experiment
LowCost-GC
Experiment-Video
| Schnellversuch zur GL- muliplikativen Verteilung

In einer einfachen Apparatur wird eine Gas- Flüssigkeits- Verteilung als multiplikative Verteilung durchgeführt. Die Gasphase ist Luft, die stationäre Phase ist Wasser. Als Substanz wird Kohlenstoffdioxid eingesetzt, dessen Anwesenheit durch einen Indikator angezeigt werden kann. |  |
|
 K01c1 K01c1
Experiment
LowCost-GC
Experiment-Video
| Kleine einführende Experimente mit dem AK LowCost-GC

Schöne kleine einleuchtende Experimente zur LowCost - Gaschromatografie.
|  |
|
 K01c2 K01c2
Experiment
LowCost-GC
Experiment-Video
| Der AKLowCost WLD (Glühbirnrchen-Sensor)

Es wird ein „geknacktes Birnchen" auf die Tauglichkeit, als WLD-Sensor zu fungieren, geprüft. |  |
|
 K02 K02
Experiment
LowCost und Medizin-Technik
| Papierchromatografie von Lebensmittelfarben bzw. Tinten

Die Papierchromatographie ist ein Trennverfahren, bei dem die Hydrathülle der Cellulosefasern die stationäre Phase bildet. Als mobile Phase dient hier Wasser. Die Methode bietet sich z.B. zur einfachen "Reinheitskontrolle" von Lebensmittelfarben an. |  |
|
 K02a K02a
Experiment
LowCost und Medizin-Technik
| Dünnschichtchromatografie von Filzstiftfarben

Die Dünnschichtchromatografie (DC) ist ein Trennverfahren, bei dem sich die dünne aus feinkörnigem Material bestehende Trennschicht (stationäre Phase) auf einer Trägerplatte aus Glas, Metall oder einer geeigneten Folie befindet. Als mobile Phase dient hier Ethanol. |  |
|
 K03 K03
Experiment
| Trennung von Blattpigmenten mit Säulenchromatografie

Die Blattfarbstoffe werden eluiert und säulenchromatografisch getrennt, sodass genügend große Mengen zu weiteren (spektroskopischen) Untersuchungen zur Verfügung stehen. |  |
|
 K03a K03a
Experiment
LowCost und Medizin-Technik
| DC Trennung von Blattpigmenten (Dünnschichtchromatographie)

Die Blattfarbstoffe werden eluiert und chromatographisch getrennt, sodass genügend große Mengen zu weiteren (spektroskopischen) Untersuchungen zur Verfügung stehen. |  |
|
 K04 K04
Experiment
AK Analytik 11
Teachers Helper
AK Analytik 32.NET
LowCost und Medizin-Technik
All-Chem-Misst
| LC-GC Trennung eines Feuerzeug-(Butangas-)Gemisches

Mit einem LowCost-Gaschromatografen ist es möglich, fast „professionelle“ Trennungen von Feuerzeuggas zu erzielen. Die Werte erscheinen auf dem Display des Messmoduls AK LCGC 04. Ein Computer ist hervorragend geeignet, die lästigen Schreib- und Zeichenarbeiten bei gas-chromatografischen Analysen zu übernehmen. Auch „Auswertungen“ werden unterstützt. |  |
|
K04b
Experiment
LowCost und Medizin-Technik
LowCost-GC
Experiment-Video
| LC-GC Mein erstes Gaschromatogramm von Feuerzeuggas

Mit einem LowCost - Gaschromatografen ist es möglich, fast 'professionelle' Trennungen von Feuerzeuggas zu erzielen. Die Wertepaare werden auf dem Display des Messmoduls z.B. des AK LCGC 04 abgelesen, Tabelle und Graph dabei 'von Hand' erstellt. Die Trennung kann auch akustisch verfolgt werden. |  |
|
K04c
Experiment
AK Analytik 32.NET
LowCost und Medizin-Technik
LowCost-GC
Experiment-Video
| LC-GC Trennung von Feuerzeug- bzw. Campinggaz

Mit einem LowCost - Gaschromatografen ist es möglich, fast „professionelle" Trennungen von Feuerzeuggas zu erzielen. Die Wertepaare werden auf dem Display des Messmoduls z. B. des AK LCGC 04 abgelesen, Tabelle und Graph dabei „von Hand" erstellt. |  |
|
K04d
Experiment
LowCost und Medizin-Technik
Selbstbau
LowCost-GC
Experiment-Video
| LC-GC Chromatogramm von Feuerzeuggas - Die Augen sind der Detektor

Beim LowCost - Gaschromatografen wird die Aquarienpumpe durch eine Wasserstoffflasche ersetzt. Die Kohlenwasserstoffe (Propan, Butan) färben die Wasserstoffflammme stark gelb ein. Es wird auch gezeigt, dass nicht jede Trennsäule gleichermassen geeignet ist. |  |
|
 K04g K04g
Experiment
AK Analytik 11
AK Analytik 32.NET
LowCost und Medizin-Technik
All-Chem-Misst
| LC-GC Einsatz in der Kriminalistik

Explosion eines Wohnhauses. War es ein Unglück (Erdgas) oder hinterhältiger Mord, verübt mit Campinggas? |  |
|
 K05 K05
Experiment
AK Analytik 11
AK Analytik 32.NET
LowCost und Medizin-Technik
LowCost-GC
| LC-GC: Fotochlorierung von Methan und Trennung der Produkte

Durch Beleuchten mit einem Halogenstrahler(500 W) aus dem Baumarkt lässt sich ein Chlor/Methan-Gemisch zur Reaktion bringen. Dieser traditionelle Versuch nach Glaser1) im Gasometer wurde für Medizintechnik-TeileA) umgearbeitet und dadurch auf Halbmikrotechnik verkleinert. |  |
|
 K06 K06
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
| GC Trennung von Leichtbenzin

Der TECHNOCHEM ist wohl der in den deutschen Schulen verbreitetste Gaschromatograph. Natürlich läßt sich nach vorheriger Anpassung die Trennung auch mit anderen Gaschromatographen, auch mit dem Modellchromatographen von K04, aufnehmen. | |
|
K07
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
| GC Bromierung von Ethen und Trennung der Produkte

Durch Bromierung lässt sich aus Ethen Dibromethan herstellen. Bromiert man allerdings Ethen in einer konzentrierten Kochsalzlösung, so lässt sich auch Bromchlorethan herstellen. Dieser Versuch soll die Leistungsfähigkeit der Gaschromatografie zeigen. Die Trennung der Reaktionsprodukte gelingt sowohl mit dem Chromatografen von Blatt K04 als auch mit dem von Arbeitsblatt K05. Entsprechend ist die jeweilige Geräteliste bzw. der Versuchsaufbau zu wählen. | |
|
K08
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
| GC Quantitative Alkoholbestimmung in Spirituosen und Kosmetika

Nach Bestimmung der Response - Faktoren lassen sich die Alkoholgehalte in Spirituosen und kosmetischen Wässerchen „halbquantitativ“ bestimmmen. | |
|
 K08ag K08ag
Experiment
AK Analytik 11
Teachers Helper
LowCost-GC
| LC GC (GS) Alkoholbestimmung in alkoholreduzierten Bieren

Durch Vergleich lassen sich die Alkoholgehalte in alkoholreduzierten Bieren „halbquantitativ" abschätzen |  |
|
 K08bg K08bg
Experiment
AK Analytik 11
Teachers Helper
LowCost-GC
| LC GC (GS) Alkoholbestimmung nach Genuss einer Praline

Versuch, den durch Genuss einer "Praline" aufgenommenen Alkohol "halbquantitativ" abschätzen. |  |
|
 K08cg K08cg
Experiment
AK Analytik 11
Teachers Helper
LowCost-GC
| LC GC (GS) Methanol im Selbstgebrannten

Die einzelnen Fraktionen bei der Destillation von selbst angesetztem Wein mit einer käuflichen "Spaßdestille" werden untersucht. |  |
|
 K08dg K08dg
Experiment
AK Analytik 11
LowCost-GC
| LC GC (GS) Alkoholgehalt bei selbsthergestelltem Apfelwein

Der Alkoholgehalt lässt sich bei der Herstellung von selbstgemachtem Apfelwein recht einfach überprüfen. |  |
|
K09
Experiment
AK Analytik 11
AK Analytik 32.NET
| GC Verfolgung der Verseifung bzw. Esterbildung von Ethansäureethylester

Nach Bestimmung der Response - Faktoren der einzelnen Komponenten, nach dem Muster von K08 lassen sich die Konzentrationen der an der Esterreaktion beteiligten Komponenten mit der Zeit verfolgen. | |
|
 K09g K09g
Experiment
AK Analytik 11
LowCost-GC
| LC GC (GS) Verfolgung der Veresterung bzw. Verseifung von Ethansäureethylester

Man lässt die beiden konkurrierenden Reaktionen bei 60°C mit einer hohen Katalysatormenge ablaufen, um die Einstellung des Gleichgewichts per GC innerhalb einer Doppelstunde verfolgen zu können. |  |
|
 K09ag K09ag
Experiment
AK Analytik 11
Teachers Helper
LowCost-GC
| LC GC (GS) Verfolgung der Veresterung bei selbst hergestelltem Apfelessig

Man stellt aus Essig-Essenz und Apfelsaft Apfelessig her und untersucht den Gasraum über längere Zeit auf seine Inhaltsstoffe.
Parallel dazu wird ein zweiter "Apfelessig" hergestellt, aber 0,5 mL Schwefelsäure zugegeben. Diese Probe wird zusätzlich auf einer Heizung etwas erwärmt.
|  |
|
 K10 K10
Experiment
AK Analytik 11
Teachers Helper
AK Analytik 32.NET
LowCost und Medizin-Technik
Selbstbau
LowCost-GC
| LC-GC Pyrolyse von PE-Folie und Identifzierung der Produkte

In einem sehr einfachen Versuch lässt sich durch Erhitzen im Reagenzglas eine Thermolyse von PE- Folie durchführen. |  |
|
 K11 K11
Experiment
AK Analytik 11
Teachers Helper
AK Analytik 32.NET
LowCost und Medizin-Technik
Selbstbau
LowCost-GC
| LC-GC Katalytische Hydrierung von Alkenen bzw. Alkinen

Durch gleichzeitiges Überleiten eines Alkens bzw. Alkins und Wasserstoff über einen geeigneten Katalysator kann die sehr eindrucksvolle Volumenabnahme bei der quantitativen Hydrierung beobachtet werden. Dabei wird eine starke Wärmetönung festgestellt Diese ist eine der wenigen Reaktionen, die auch ohne Zufuhr von "Aktivierungsenergie" spontan ablaufen und Schüler die Katalysatorwirkung unmittelbar erfahren lassen. |  |
|
 K12 K12
Experiment
AK Analytik 11
Teachers Helper
AK Analytik 32.NET
LowCost und Medizin-Technik
LowCost-GC
| LC-GC Thermisches bzw. katalytisches Cracken von Propan

In einer sehr einfachen „Universellen Kolbenpoberapparatur" lässt sich je nach Versuchsbedingung das katalytische Cracken bzw. das Dehydrieren von Propan bzw. Butan durchführen. |  |
|
 K13 K13
Experiment
AK Analytik 11
LowCost und Medizin-Technik
LowCost-GC
| LC-GC Chlorierung von Ethen

Die Addition von Chlor an ungesättigte Verbindungen lässt sich über einen Zeitraum verfolgen. Es kann gezeigt werden, dass Ethen sich im Gegensatz zu Ethan (Methan) auch ohne Licht halogenieren lässt. Es wurde Chlor gewählt, da man die Reaktion leichter quantitativ verfolgen kann als die mit Bromdampf. Die für die Reaktion benötigten Gase werden direkt in der Apparatur erzeugt. |  |
|
K14
Experiment
AK Analytik 11
Teachers Helper
LowCost und Medizin-Technik
Selbstbau
LowCost-GC
| LC-GC Ethen beim Reifen von Äpfeln

Ein Apfel wird in zwei Hälften geschnitten und in das „Reifeglas“ gegeben. Zu bestimmten Zeiten kann von dem umgebenden Gas ein Chromatogramm aufgenommen werden. |  |
|
 K14g K14g
Experiment
AK Analytik 11
Teachers Helper
LowCost und Medizin-Technik
Selbstbau
LowCost-GC
| LC-GC (GS) Ethen beim Reifen von Äpfeln

Ein Apfel wird mit dem Messer leicht eingeschnitten und in das „Reifeglas" gegeben. Zu bestimmten Zeiten kann von dem umgebenden Gas ein Chromatogramm aufgenommen werden. |  |
|
 K16 K16
Experiment
LowCost und Medizin-Technik
LowCost-GC
| LC-GC: Gasherstellung mit vielen Varianten

Unterschiedlichste Apparaturen zur Gasherstellung |  |
|
 K17 K17
Experiment
AK Analytik 11
Teachers Helper
LowCost und Medizin-Technik
Selbstbau
LowCost-GC
| LC-GC: Herstellung von Biogas

Biogas ist zurzeit in aller Munde; doch die Erzeugung ist nicht ganz so leicht, wie es scheint.
Die Herstellung gelingt allerdings gut, wenn man sich Gärsubstrat besorgt. Die stabilen Bakterien lassen sich mit Küchenabfällen etc. füttern.
|  |
|
 K18 K18
Experiment
AK Analytik 11
Teachers Helper
LowCost und Medizin-Technik
Selbstbau
LowCost-GC
| LC-GC: Herstellung von Biowasserstoff

Aus Zuckerrübenschnitzeln und Gartenerde und 80 °C heißem Wasser entsteht ein Gasgemisch. Dieses enthält so viel Biowasserstoff, dass ohne Gaswäsche eine Brennstoffzelle betrieben werden kann, die einen Flügelmotor mit Strom versorgt!! |  |
|
 L01 L01
Experiment
| Organische Chemie: Qualitative Organische Elementaranalyse

Im allgemeinen wird eine einfache Prüfung auf Kohlenstoff, Wasserstoff und Stickstoff, seltener auf Halogene, Schwefel, Phosphor oder andere Elemente durchgeführt. |  |
|
 L01a L01a
Experiment
| Einfache Qualitative Organische Elementaranalyse (Brenngase - nur: C und H)

Im allgemeinen wird eine einfache Prüfung auf Kohlenstoff, Wasserstoff durchgeführt. |  |
|
 L01b L01b
Experiment
| Einfache Qualitative Organische Elementaranalyse (Alkohol - nur: C und H)

Im allgemeinen wird eine einfache Prüfung auf Kohlenstoff, Wasserstoff durchgeführt. |  |
|
 L02 L02
Experiment
| Quantitative organische Elementaranalyse nach Liebig

Die Elementaranalyse ist ein Verfahren zur Bestimmung der quantitativen Zusammensetzung eines Stoffes. | 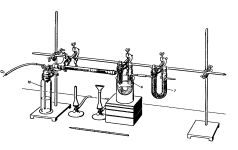 |
|
 L03 L03
Experiment
| Vereinfachte Quantitative Elementaranalyse nach Rinschen

Die Liebig- Analyse wird so vereinfacht, daß nur das Reaktionsprodukt Wasser aufgefangen wird. Falls die Substanz nur C, H und O enthält, wird der Anteil an C ebenfalls berechnet | 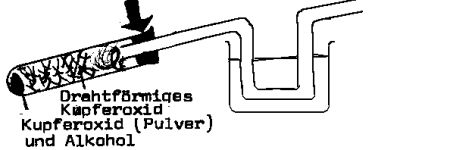 |
|
 L04 L04
Experiment
| Vereinfachte Quantitative Elementaranalyse (nur Kohlenstoff)

Die Substanz wird mit festem Kupferoxid oxidiert. Man geht bei der Reaktion davon aus, daß als einziger gasförmiger Stoff Kohlenstoffdioxid entsteht. Das entstehende Wasser kondensiert. Die Volumina der festen und flüssigen Stoffe (kondensiertes Wasser) werden vernachlässigt | 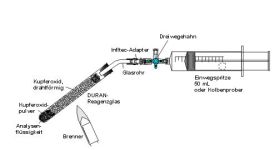 |
|
 L05 L05
Experiment
| Quantitative Halogenanalyse nach Schöninger

Die chlorhaltige Substanz wird verbrannt, wobei Chlorwasserstoff entsteht. Da Chlorwasserstoff sich leicht in Wasser löst, kann man die entstehenden Chloridionen durch Titration mit Silber- Ionen bestimmen. | 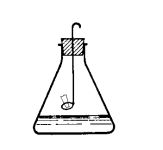 |
|
 L06 L06
Experiment
| Quantitative Kohlenstoffanalyse bei Gasen, die kein N und S enthalten

Die Substanz wird mit festem Kupferoxid oxidiert. Man geht bei der Reaktion davon aus, daß als einziger gasförmiger Stoff Kohlenstoffdioxid entsteht. Aus jedem Kohlenstoffatom entsteht ein Kohlendioxidmolekül. Nach Avogadro bleibt damit das Volumen konstant (C=1) oder es kommt zu einer ganzzahligen Vervielfachung des Ausgangsvolumens. So müssen zum Beispiel aus 1 mol Propan 3 mol Kohlendioxid entstehen. | 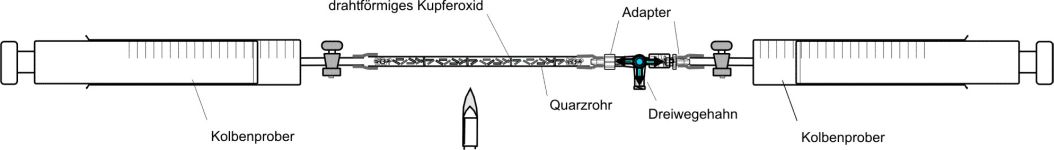 |
|
 L06a L06a
Experiment
| Anzahl der "H"-Atome bei Kohlenwasserstoffen

Bei geschickter Versuchsführung kann man durch Zersetzen eines Kohlenwassertsoffs an Aktivkohle den Wasserstoff fast quantitativ abspalten. Der Verlauf der Reaktion kann mit der Gaschromatographie verfolgt werden. | 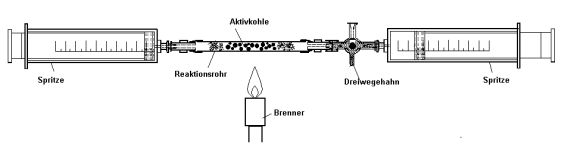 |
|
 L07 L07
Experiment
| Bestimmung der Molmasse von leicht verdampfbaren Flüssigkeiten (Schüttel-Meyer)

Diese "Methode" ist geeignet für flüchtige Stoffe mit einem Siedepunkt bis etwa 75 °C. Ein bestimmtes Volumen einer Flüssigkeit mit bekannter Dichte wird in einem Kolben durch Schütteln verdampft, um in den Geltungsbereich des Gesetzes von Avogadro zu kommen. | 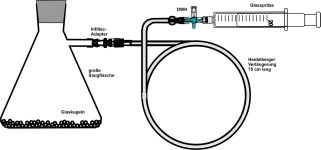 |
|
 L07a L07a
Experiment
| Bestimmung der Molmasse von leicht verdampfbaren Flüssigkeiten (Schüttel-Meyer)

Diese "Methode" ist geeignet für flüchtige Stoffe mit einem Siedepunkt bis etwa 75 °C. Ein bestimmtes Volumen einer Flüssigkeit mit bekannter Dichte wird in einem Kolben durch Schütteln verdampft, um in den Geltungsbereich des Gesetzes von Avogadro zu kommen. | 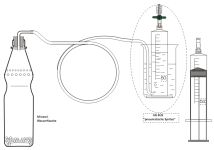 |
|
 L08 L08
Experiment
| Bestimmung der Molmasse (Heizofenmethode)

Die Methode ist geeignet für flüchtige Stoffe mit einem Siedepunkt bis etwa 250 °C. Man gibt ein bestimmtes Volumen einer Flüssigkeit mit bekannter Dichte in einen Kolben und verdampft die Flüssigkeit, um in den Geltungsbereich des Gesetzes von Avogadro zu kommen. | 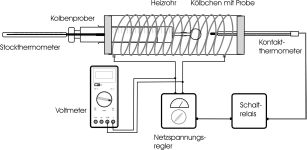 |
|
 L09 L09
Experiment
| Bestimmung der Siedetemperatur

Im Experiment stellt man die Siedetemperatur meist durch Destillation fest, bei der man das Siedeintervall der Substanz feststellt. Die Literaturwerte der Siedetemperatur einer Substanz sind häufig verschieden, weil die Versuche leicht ungenau werden . | |
|
 L10 L10
Experiment
| Bestimmung der Schmelztemperatur

In der Praxis wird bei einfachen Bestimmungen meist das Schmelzintervall aufgenommen und die Schmelztemperatur nach mehreren Versuchswiederholungen ermittelt . | 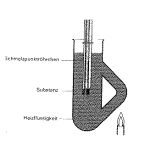 |
|
 L11 L11
Experiment
| Bestimmung der Dichte

Der Quotient aus Masse und Volumen eines Stoffes ist als Dichte definiert. Die Dichte dient als Kriterium für die Reinheit eines Stoffes. |  |
|
 L12 L12
Experiment
| Bestimmung des Brechungsindexes (Refraktometrie)

In der Refraktrometrie benutzt man den Brechungsindex (n) um flüssige Substanzen zu identifizieren oder um deren Reinheit zu prüfen. Der Brechungsindex ist stark temperaturabhängig und durch verschiedene Wellenlängen des Lichtes veränderbar. Aus diesem Grund werden die Temperatur und die Wellenlängen als Indizes am Brechungsindex vermerkt z.B. n20d (20 Grad und die D-Linie, 589 nm). |  |
|
 L13 L13
Experiment
| Polarimetrie

Es gibt Verbindungen, in denen die Moleküle asymmetrisch gebaut sind. Diese Verbindungen sind "optisch aktiv", d.h., daß sie die Schwingungsebene von linear polarisiertem Licht um einen Drehwinkel (a) drehen können, wenn sie von diesem Licht durchstrahlt werden. Diese Drehung der Polarisationsebene kann nach rechts (+) und auch nach links (-) erfolgen. Die Konzentration c (g/ 100mL Lsg.), die Temperatur, die Schichtdicke l (dm) und die Wellenlänge (l) beeinflussen die Drehung | |
|
 M01a M01a
Experiment
| Messungen des Stroms: Bestimmung der Faraday-Konstanten

Verdünnte Kalilauge wird zwischen zwei Eisenelektroden mit konstanter Stromstärke elektrolysiert. Das entstehende Knallgas verdrängt dabei eine entsprechende Menge Kalilauge aus dem Elektrolyserohr. Das Volumen wird gemessen und mit der geflossenen Ladung in Relation gesetzt. | 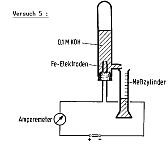 |
|
 M01b M01b
Experiment
LowCost und Medizin-Technik
Selbstbau
Selbstbau-Video
Experiment-Video
| Elektrolyse im Krautsalatbecher -Faraday-Konstante - LowCost

Variante der Hoffman-Elektrolyse: Verdünnte Kalilauge an zwei Eisenelektroden in getrennten Gefäßen mit konstanter Stromstärke elektrolysiert. Die entstehenden Gase Wasserstoff und Sauerstoff verdrängen dabei ein entsprechendes Volumen Kalilauge aus den Elektrolysiergefäßen. Die Volumina werden gemessen und mit der geflossenen Ladung in Relation gesetzt. |  |
|
 M01c M01c
Experiment
| Wasserelektrolyse mit Brennstoffzelle

Moderne Brennstoffzellen machen‘s möglich: Hier wird nicht gepfuscht- sondern destilliertes Wasser elektrolysiert. Hier wird ein käuflicher Elektrolyseur eingesetzt |  |
|
 N01 N01
Experiment
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| U-I: Aufnahme einer Strom- Spannungskurve einer Glühbirne

In dieser Vorübung (Variante zu Arbeitsblatt D01) wird eine elektrische Schaltung zur Messung von Spannung und Stromstärke beim Betrieb eines Lämpchens aufgebaut und betrieben. Dabei werden die Messmethoden, Schaltungsaufbauten und Zusammenhänge zwischen Spannung, Stromstärke, Widerstand, Leitwert und Leistung für spätere chemische Untersuchungen eingeübt. Zur Messung der elektrischen Leitfähigkeit von Lösungen wird das Lämpchen später gegen einen Leitfähigkeitsprüfer ausgetauscht und mit einer konstanten Wechselspannung betrieben. |  |
|
 N01a N01a
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| U-I Elektrolyse - Aufnahme einer Strom- Spannungskurve-Salzsäure

Salzsäure wird zwischen zwei Platinelektroden elektrolysiert. Dabei wird mit U = 0 V beginnend die Elektrolysierspannung ständig erhöht und die zugehörige Stromstärke gemessen. Die Zersetzungsspannung wird ´grafisch´ ermittelt |  |
|
 N01b N01b
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
AK Analytik 32.NET
All-Chem-Misst
| U-I Elektrolyse - Aufnahme einer Strom- Spannungskurve-Schwefelsäure

Schwefelsäure wird zwischen zwei Platinelektroden elektrolysiert. Dabei wird mit U = 0 V beginnend die Elektrolysierspannung ständig erhöht und die zugehörige Stromstärke gemessen. Die Zersetzungsspannung wird ´grafisch´ ermittelt |  |
|
 N01c N01c
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| U-I: Wasserlektrolyse ohne Pfusch (Elektrolyseur-Kennlinie)

Destilliertes Wasser wird wie bei Arbeitsblatt M01C ohne Zusätze, wie Schwefelsäure (Arbeitsblatt M01A), in einer reversiblen Brennstoffzelle bzw. in einem käuflichen Elektrolyseur in die Elemente zerlegt (Arbe. Dabei wird mit U = 0 V beginnend die Elektrolysierspannung ständig erhöht und die zugehörige Stromstärke gemessen. Die im Strom-Spannungs-Diagramm entstehende "Kennlinie" kann diskutiert werden. Ebenso kann die Leistung des Elektrolyseurs in Abhängigkeit von der Spannung ermittelt werden. |  |
|
 N01d N01d
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| U-I: Kennlinie einer Brennstoffzelle

Die Spannung einer Brennstoffzelle soll bei unterschiedlicher Belastung (unterschiedliche Lastwiderstände) untersucht werden. Bei der Kennlinie der Brennstoffzelle sind im Gegensatz zum Elektrolyseur U und I vertauscht. |  |
|
 N01e N01e
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| U-I: Kennlinie eines Solarmoduls

Es soll ermittelt werden, wie bei einem Solarmodul Strom und Spannung voneinander abhängen. |  |
|
 N01f N01f
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| U-I: Der didaktische Wunderakku im Einsatz

Hier werden bei dem schönen Versuch vom Arbeitsblatt N03A (Zinkiodidakku) Spannung und Strom gemessen, um die Deutungen zu vertiefen. |  |
|
 N02a N02a
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| pH-LF: Titration von HCl mit NaOH - Tastendruck

Da sich bei der Neutralisation die Leitfähigkeit und der pH-Wert ändern, kann man die Titration sowohl konduktometrisch wie auch potentiometrisch verfolgen. Mit dem ALL-CHEM-MISST hat man die Möglichkeit, Leitfähigkeit und pH-Wert gleichzeitig aufzunehmen.
Die Messwertaufnahme erfolgt über Tastendruck. |  |
|
 N02b N02b
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
| pH-LF: Titration von HCl mit NaOH - Gleichlaufbürette

Hier wird gezeigt, wie man mit dem ALL-CHEM-MISST/AK-Analytik32.NET auch (Mehrkanal-)Titrationen durchführen kann. Die Lauge wird mit Hilfe einer AK-Gleichlaufbürette zugegeben und die Titration so automatisiert. Natürlich sind in analoger Weise auch Einkanalmessungen für pH, LF T oder U möglich |  |
|
 N02c N02c
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
| pH-LF: Titration von HCl mit NaOH - AK-Motorbürette

Hier soll beispielhaft gezeigt werden, wie man mit der Kombination ALL-CHEM-MISST / AK-Analytik32.NET auch (Mehrkanal-)Titrationen durchführen kann. Die Lauge wird mit Hilfe einer AK-Motorbürette zugegeben und die Titration so automatisiert. Natürlich sind in analoger Weise auch Einkanalmessungen für pH, LF T oder U möglich. |  |
|
N02d
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
| pH-LF: Titration von HCl mit NaOH - Motorkolbenbürette (T80)

Hier soll beispielhaft gezeigt werden, wie man mit der Kombination ALL-CHEM-MISST / AK-Analytik32.NET auch (Mehrkanal-)Titrationen durchführen kann. Die Lauge wird mit Hilfe der Schott- Motorkolbenbürette T80 zugegeben und die Titration so automatisiert. Natürlich sind in analoger Weise auch Einkanalmessungen für pH, LF T oder U möglich. |  |
|
 N02e N02e
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
| pH-LF: Titration von HCl mit NaOH - Waagenbürette

Hier soll beispielhaft gezeigt werden, wie man mit der Kombination ALL-CHEM-MISST / AK-Analytik32.NET auch (Mehrkanal-)Titrationen durchführen kann. Die Lauge wird mit Hilfe einer AK-Waagenbürette zugegeben und die Titration so automatisiert. Natürlich sind in analoger Weise auch Einkanalmessungen für pH, LF T oder U möglich. . |  |
|
 N02f N02f
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
| pH-LF: Titration von HCl mit NaOH - AK-FM04 (Tropfenzähler)

Hier soll beispielhaft gezeigt werden, wie man mit der Kombination ALL-CHEM-MISST / AK-Analytik32.NET auch (Mehrkanal-)Titrationen durchführen kann. Die Lauge wird mit Hilfe einer Bürette zugegeben, mit dem AK-Tropfenzähler gemessen und die Titration so automatisiert. Natürlich sind in analoger Weise auch Einkanalmessungen für pH, LF T oder U möglich. |  |
|
N03
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
| m-T: Verdunsten von Ether und anderen niedrig siedenden Flüssigkeiten

Ein Wattebausch wird mit einer Flüssigkeit getränkt.. Die verdunstende Flüssigkeit führt zu einem Massenverlust und einer Temperaturänderung. Beide Größen werden über eine bestimmte Zeit verfolgt. |  |
|
 N04a N04a
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
| LF-T: Temperaturabhängigkeit der elktr. Leitfähigkeit bei Salzsäure

Hier soll die Leitfähigkeit (ohne Temperaturkompensation) bei einem starken Elektrolyten in Abhängigkeit von der Temperatur verfolgt werden. | |
|
 N04b N04b
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
| LF-T: Temperaturabhängigkeit der elktr. Leitfähigkeit bei Essigsäure

Hier soll die Leitfähigkeit (ohne Temperaturkompensation) bei einem schwachen Elektrolyten in Abhängigkeit von der Temperatur verfolgt werden. | |
|
 N05 N05
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| T-T: Schmelzen / Abkühlen von Natriumthiosulfat

Die Temperaturänderung beim Schmelzen von Natriumthiosulfat bzw. beim Auskristallisieren der unterkühlten Schmelze wird gemessen und mit dem Temperaturverhalten von Wasser verglichen. Die Begriffe Schmelztemperatur, Schmelzwärme, Kristallisationspunkt, Kristallisationswärme und unterkühlte Schmelze können erläutert werden. Praktische Anwendungen: „Wärmekissen“, Schutz der Baumblüte bei Frost. |  |
|
 N05a N05a
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
| T-T: Modellversuch zum Treibhauseffekt

Die Temperaturänderung bei der Beleuchtung zweier Bechergläser, die zum Teil mit Tonpapier ausgekleidet sind und einmal Luft, zum anderen Kohlenstoffdioxid enthalten, soll über eine gewisse Zeit verfolgt werden. Dabei heizt sich das Becherglas mit Kohlenstoffdioxid schneller auf. Der Effekt wird verstärkt, wenn man den Deckel wegläßt. Das Modell ist dann wegen der unterschiedlichen Konvektionen bzw. Dichteverhältnisse nicht mehr korrekt! |  |
|
 N05b N05b
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
| T-T: Modellversuch zur Bergmannschen Regel

Die Temperaturänderung zweier mit heißem Wasser gefüllter unterschiedlich großer Kolben soll über eine gewisse Zeit verfolgt werden. |  |
|
N05c
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
| T-T-T-T: Fraktionierte Destillation von Erdöl

In einer für die Schule konstruierten Apparatur wird der Beginn einer fraktionierenden Destillation von "echtem" Erdöl nachempfunden und der Temperaturverlauf gemessen. |  |
|
 N06 N06
Experiment
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| I-d: Solarmodul: Abhängigkeits des Fotostroms vom Abstand

Es soll untersucht werden, ob und wie der Fotostrom eines Solarmoduls sich mit zunehmender Entfernung von einer Lichtquelle ändert. |  |
|
 N07 N07
Experiment
AK Analytik 11
Teachers Helper
AK Multiadapter
Multiadapter TH
AK Analytik 32.NET
All-Chem-Misst
| I-a: Solarmodul: Abhängigkeits des Fotostroms vom Winkel

Es soll untersucht werden, ob und wie der Fotostrom eines Solarmoduls sich mit zunehmendem Winkel von einer Lichtquelle ändert. |  |
|
 N10 N10
Experiment
AK Analytik 11
AK Analytik 32.NET
All-Chem-Misst
| Gaskonzentrationen beim Brennen einer Kerze

Mit Hilfe von "Vernier"-Gassensoren wird beim Brennnen einer Kerze die Luft im Verbrennungsraum untersucht. Die Konzentrationen von Sauerstofff und Kohlenstoffdioxid werden über die Zeit verfolgt. | |
|
 O01 O01
Experiment
All-Chem-Misst
All-Chem-Misst ohne Rechner
| ACMII: Zeitmessung - Kühlschrankprinzip

Butan oder Feuerzeuggas wird komprimiert und dadurch verflüssigt. Danach wird durch Entspannen die Flüssigkeit wieder gasförmig. Die Temperaturänderung wird ohne Computer mit dem ALL-CHEM-MISST auf komfortable Art und Weise digital und graphisch registriert. |  |
|
 O01a O01a
Experiment
All-Chem-Misst
All-Chem-Misst ohne Rechner
| ACMII: Langzeitmessung - Raumtemperatur

Der All-Chem-Misst ist ohne Computer in gewissem Umfang auch für Langzeitmessungen geeignet. Hier soll die Raumtemperatur über mehrere Tage aufgenommen werden. |  |
|
 O02 O02
Experiment
All-Chem-Misst
All-Chem-Misst ohne Rechner
| ACMII + Hand- bzw. Fußtaster, Beispiel: pH-Titration

Bei der Neutralisation ändert sich der pH-Wert. Die pH-Wertänderung wird mit dem ALL-CHEM-MISST auf komfortable Art und Weise digital und graphisch registriert. |  |
|
 O03 O03
Experiment
All-Chem-Misst
All-Chem-Misst ohne Rechner
| ACMII + AK-Tropfenzähler, Beispiel: pH-Titration

Bei der Neutralisation ändert sich der pH-Wert. Die pH-Wertänderung wird mit dem ALL-CHEM-MISST auf komfortable Art und Weise digital und graphisch registriert. Der AK-Tropfenzähler ermöglicht es, die Titration zu automatisieren |  |
|
 O04 O04
Experiment
All-Chem-Misst
All-Chem-Misst ohne Rechner
| ACMII + AK-Motorbürette, Beispiel: pH-Titration

Bei der Neutralisation ändert sich der pH-Wert. Die pH-Wertänderung wird mit dem ALL-CHEM-MISST auf komfortable Art und Weise digital und graphisch registriert. Die AK-Motorbürette ermöglicht es, die Titration zu automatisieren |  |
|
 O05 O05
Experiment
All-Chem-Misst
All-Chem-Misst ohne Rechner
| ACMII + Sartorius-Waage, Beispiel: pH-Titration

Bei der Neutralisation ändert sich der pH-Wert. Die pH-Wertänderung wird mit dem ALL-CHEM-MISST auf komfortable Art und Weise digital und graphisch registriert. Die AK Waagenbürette ermöglicht es, in Kombination mit einer Sartorius-Waage die Titration zu automatisieren. |  |
|
 O06 O06
Experiment
All-Chem-Misst
All-Chem-Misst ohne Rechner
| ACMII + AK-Gleichlaufbürette, Beispiel: pH-Titration

Bei der Neutralisation ändert sich der pH-Wert. Die pH-Wertänderung wird mit dem ALL-CHEM-MISST auf komfortable Art und Weise registriert. Mit der AK-Gleichlaufbürette kann man die Titration automatisieren. |  |
|
















































































































































































































