2. Qualitative Analyse von Wasser
A. Nachweis von Sauerstoff
Aus der Klasse 7 wissen wir, dass man Sauerstoff mit der Glimmspanprobe nachweist.
Bei Wasser ist das Ergebnis der Glimmspanprobe Negativ.
Magnesium reagier heftiger als Holz mit (Luft-)Sauerstoff unter Ausbildung von weißer Magnesiumasche. Die Flamme ist grellweiß.
Da man Magnesium nur schlecht unter Wasser anzünden kann wollen wir es in Wasserdampf entzünden. Aber alle Luft muss vorher raus.
Versuchsaufbau:
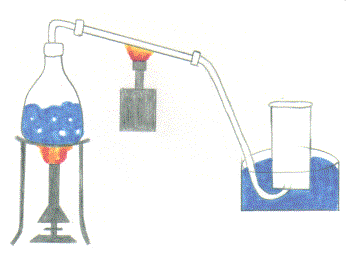
Durchführung:
Wir erhitzen mit Brenner 1 das Wasser und warten bis alle Luft raus ist (Es gibt keine Bläschen mehr in der pneumatischen Wanne. Dann füllen wir den Standzylinder erneut mit Wasser. Wir zünden Brenner 2 an und erhitzen das Magnesium. Es verbrennt mit gleißender Flamme. Nach dem Abkühlen sehen wir im Reaktionsrohr ein weißes Pulver (Magnesia). Das ist der Nachweis von Sauerstoff im Wasser.
B. Nachweis von Wasserstoff
Im Zylinder sammelt sich ein farbloses Gas. Es muss gleichzeitig bei der Bildung der Reaktion des Magnesiums mit (aus) dem Wasser entstanden sein.
Mit der Knallgasprobe ("Plop" bzw. "Puii") identifizieren wir es als Wasserstoff.
Ergebnis:
In Wasser sind mindestens Wasserstoff und Sauerstoff enthalten.
Durchführung des gleichen Versuchs mit Teilen aus unserem Zinsser - Mini-Labor (Schrank 8)
Sofort anfangen - Versuch dauert
die ganze Schulstunde!
